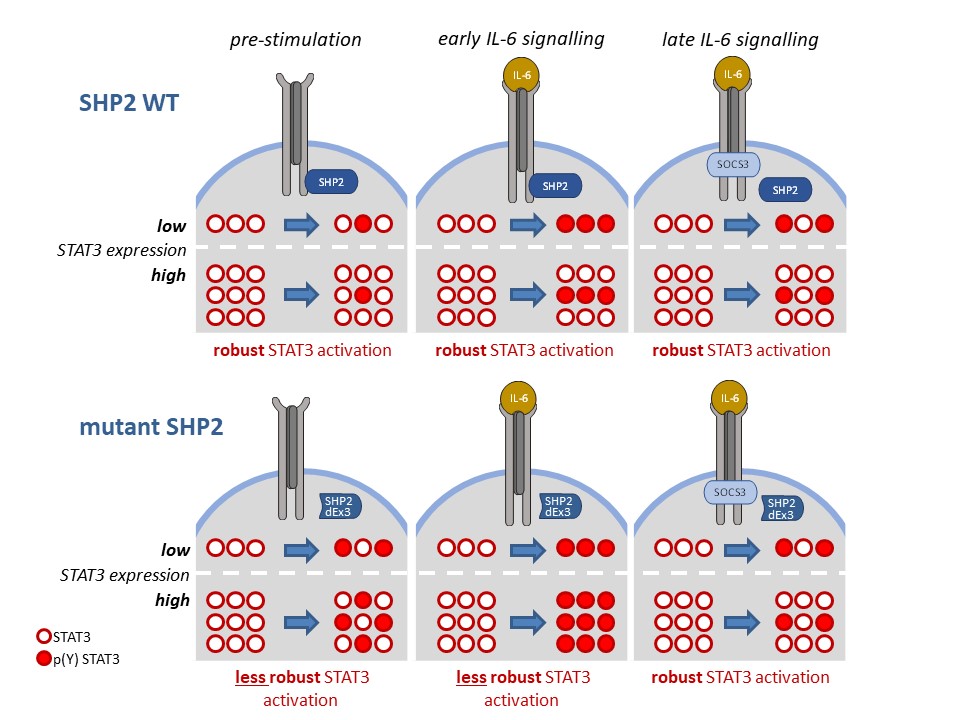
Robustheit der IL-6 Signaltransduktion
Kommunikation zwischen Zellen ist essentiell für alle physiologischen und pathophysiologischen Prozesse vielzelliger Organismen. Die Informationstheorie nach Shannon charakterisiert die Informationsübertragung in künstlichen und natürlichen Kommunikationssystemen. Hierbei wird untersucht, wie Information von einem Sender über einen rauschenden Kanal zu einem Empfänger übertragen wird. Wir nutzen dieses Modell, um die IL-6-induzierte Signaltransduktion genauer zu charakterisieren. Hierbei wird IL-6 als Sender interpretiert. Es bindet an Rezeptoren auf der Zelloberfläche und aktiviert intrazelluläre Signalkaskaden (= Kanal). Diese Signalkaskaden resultieren in der Aktivierung spezifischer Transkriptionsfaktoren, die die Transkription (Produktion von mRNA) von Zielgenen regulieren (= Empfänger). Diese Zielgene sind Grundlage für zelluläre Reaktionen. Dieser Informationskanal wird durch zelluläre Heterogenität beeinflusst. Genetisch identische Zellen innerhalb eines Organismus sind elbst innerhalb eines Organs nicht gleich. Sie unterscheiden sich z.B. massiv in der Anzahl und Aktivierung von Rezeptoren, Signalproteinen und Zielgenen. Zusätzlich entstehen durch Diffusion der Zytokine Konzentrationsgradienten.
Vor diesem Hintergrund untersuchen wir in diesem, durch den Innovationsfond der OvGU geförderten Projekt, die Konsequenzen der zellulären Heterogenität auf die Signaltransduktion und versuchen zu verstehen welche molekularen Mechanismen evolviert sind um Robustheit gegenüber zellulärer Heterogenität zu gewährleisten oder sogar Vorteile aus der Heterogenität zu ziehen. Wir nutzen dazu komplexe multiparametrische durchflusszytometrische Analysen der Aktivierung und Expression von Signalproteinen und der Expression von Zielgen mRNAs. Die Informationstheoretische Analyse erfolgt in Kooperation Michal Komorowski (Polish Academy of Sciences).